ARN missatger amb nucleòsids modificats
Un ARN missatger amb nucleòsids modificats (ARNmod, o en anglès modRNA) és un ARN missatger (ARNm) sintètic en el qual alguns nucleòsids són substituïts per altres nucleòsids modificats naturalment o per anàlegs de nucleòsids sintètics.[1] L'ARNmod s'utilitza per induir la producció d'una proteïna desitjada en determinades cèl·lules. Una aplicació important és el desenvolupament de vacunes d'ARNm, les primeres de les quals van ser aprovades com a vacunes contra la COVID-19 (per exemple, la vacuna de Pfizer–BioNTech i la vacuna de Moderna).
L'ARNm es produeix sintetitzant una cadena d'àcid ribonucleic (ARN) a partir de blocs de construcció de nucleòtids segons una plantilla d'àcid desoxiribonucleic (ADN), un procés que s'anomena transcripció.[2] Quan els blocs de construcció proporcionats a l'ARN polimerasa inclouen nucleòsids no estàndards com la pseudouridina, - en lloc dels nucleòsids d'adenosina, citidina, guanosina i uridina estàndard -, l'ARNm resultant es descriu com a modificat per nucleòsids.[3]
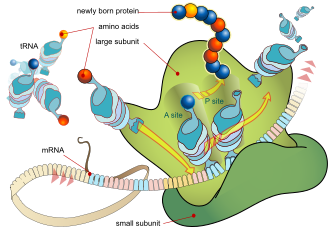
La producció de proteïnes s'inicia amb l'assemblatge de ribosomes sobre l'ARNm, que serveix després com a pla per a la síntesi de proteïnes especificant la seqüència d'aminoàcids basada en el codi genètic en el procés de biosíntesi de proteïnes anomenat traducció.[4]
Visió general
modificaPer induir les cèl·lules a produir proteïnes que normalment no produeixen, és possible introduir ARNm heteròleg al citoplasma de la cèl·lula, saltant-se la necessitat de transcripció. Per assolir aquest objectiu, però, s'ha d'evitar els sistemes cel·lulars que impedeixen la penetració i la traducció de l'ARNm estrany. Hi ha enzims gairebé omnipresents anomenats ribonucleases que descomponen l'ARNm no protegit.[5] També hi ha barreres intracel·lulars contra l'ARNm estrany, com ara els receptors del sistema immunitari innats, els receptors de tipus Toll TLR7 i TLR8, situats a les membranes endosomals. Els sensors d'ARN com TLR7 i TLR8 poden reduir dràsticament la síntesi de proteïnes a la cèl·lula, desencadenar l'alliberament de citocines com l'interferó i el TNF-alfa i, quan són prou intensos, condueixen a la mort cel·lular programada.[6]
La naturalesa inflamatòria de l'ARN exogen es pot emmascarar modificant els nucleòsids en l'ARNm.[7] Per exemple, la uridina es pot substituir per un nucleòsid similar com la pseudouridina (Ψ) o la N1-metil-pseudouridina (m1Ψ),[8] i la citosina es pot substituir per la 5-metilcitosina. Alguns d'aquests, com la pseudouridina i la 5-metilcitosina, es produeixen de forma natural en els eucariotes.[9] La inclusió d'aquests nucleòsids modificats altera l'estructura secundària de l'ARNm, que pot reduir el reconeixement pel sistema immunitari innat alhora que permet una traducció efectiva.[10]
Importància de les regions no traduïdes
modificaUn ARNm normal comença i acaba amb seccions que no codifiquen els aminoàcids de la proteïna real. Aquestes seqüències als extrems 5′ i 3′ d'una cadena d'ARNm s'anomenen regions no traduïdes (UTR). Els dos UTR en els seus extrems de cadena són essencials per a l'estabilitat d'un ARNm i també d'un ARNmod, així com per a l'eficiència de la traducció, és a dir, per la quantitat de proteïna produïda. En seleccionar UTR adequats durant la síntesi d'un ARNmod, es pot optimitzar la producció de la proteïna diana a les cèl·lules diana.[11][12]
Lliurament
modificaHi ha diverses dificultats en la introducció de ARNmod en determinades cèl·lules diana. En primer lloc, cal protegir el ARNmod de les ribonucleases.[13] Això es pot aconseguir, per exemple, embolicant-lo en liposomes. Aquest "embalatge" també pot ajudar a garantir que el modRNA s'absorbeixi a les cèl·lules diana. Això és útil, per exemple, quan s'utilitza en vacunes, ja que les nanopartícules són captades per cèl·lules dendrítiques i macròfags, que tenen un paper important en l'activació del sistema immunitari.[14]
A més a més, pot ser desitjable que l'ARNmod aplicat s'introdueixi en cèl·lules específiques del cos. Aquest és el cas, per exemple, si s'estimula la multiplicació de les cèl·lules musculars del cor. En aquest cas, l'ARNmod empaquetat es pot injectar directament en una artèria com una artèria coronària.[15]
Aplicacions
modificaCom s'ha dit abans, un camp d'aplicació important són les vacunes amb ARNm, de les quals les primeres autoritzades per al seu ús en humans van ser les vacunes COVID-19 per tractar el SARS-CoV-2.[16][17][18][19][20][21][22] Alguns exemples de vacunes contra la COVID-19 que utilitzen ARNmod inclouen els desenvolupats per la cooperació de BioNTech/Pfizer/Fosun International (BNT162b2) i per Moderna (mRNA-1273).[23][24][25] La vacuna de CureVac contra la COVID-19, però, utilitza ARN no modificat.[26]
Altres possibles usos de l'ARNmod inclouen la regeneració del teixit muscular cardíac danyat[27][28] i la teràpia contra el càncer.[29][30]
Referències
modifica- ↑ «Synthetic chemically modified mRNA (modRNA): toward a new technology platform for cardiovascular biology and medicine». Cold Spring Harbor Perspectives in Medicine, 5, 1, 10-2014, pàg. a014035. DOI: 10.1101/cshperspect.a014035. PMC: 4292072. PMID: 25301935.
- ↑ From DNA to RNA. 4. Garland Science, 2002.
- ↑ «Nucleoside Modified mRNA Vaccines for Infectious Diseases». A: RNA Vaccines. 1499, 2017, p. 109–121 (Methods in Molecular Biology). DOI 10.1007/978-1-4939-6481-9_6. ISBN 978-1-4939-6479-6.
- ↑ The Three Roles of RNA in Protein Synthesis. 4th. Nova York: W. H. Freeman, 2000, p. Sec 4.4.
- ↑ RNA Biology, 9, 11, 11-2012, pàg. 1319–30. DOI: 10.4161/rna.22269. PMC: 3597572. PMID: 23064118.
- ↑ RNA Biology, 9, 6, 6-2012, pàg. 828–42. DOI: 10.4161/rna.20206. PMC: 3495747. PMID: 22617878.
- ↑ Karikó, K; Buckstein, M; Ni, H; Weissman, D Immunity, 23, 2, 8-2005, pàg. 165–75. DOI: 10.1016/j.immuni.2005.06.008. PMID: 16111635.
- ↑ Journal of Controlled Release, 217, 2015, pàg. 337–344. DOI: 10.1016/j.jconrel.2015.08.051. PMID: 26342664.
- ↑ Nucleic Acids Research, 44, 2, 1-2016, pàg. 852–62. DOI: 10.1093/nar/gkv1182. PMC: 4737146. PMID: 26578598.
- ↑ Nucleic Acids Research, 45, 10, 6-2017, pàg. 6023–6036. DOI: 10.1093/nar/gkx135. PMC: 5449617. PMID: 28334758.
- ↑ RNA Biology, 9, 11, 11-2012, pàg. 1319–30. DOI: 10.4161/rna.22269. PMC: 3597572. PMID: 23064118.
- ↑ Molecular Therapy, 27, 4, 4-2019, pàg. 824–836. DOI: 10.1016/j.ymthe.2018.12.011. PMC: 6453560. PMID: 30638957.
- ↑ RNA Biology, 9, 11, 11-2012, pàg. 1319–30. DOI: 10.4161/rna.22269. PMC: 3597572. PMID: 23064118.
- ↑ Vaccine, 32, 3, 1-2014, pàg. 327–37. DOI: 10.1016/j.vaccine.2013.11.069. PMID: 24295808 [Consulta: free].
- ↑ Molecular Therapy. Methods & Clinical Development, 9, 6-2018, pàg. 330–346. DOI: 10.1016/j.omtm.2018.04.003. PMC: 6054703. PMID: 30038937.
- ↑ «Pfizer and BioNTech Celebrate Historic First Authorization in the U.S. of Vaccine to Prevent COVID-19». , 12-12-2020.
- ↑ The New England Journal of Medicine, 383, 27, 12-2020, pàg. 2603–2615. DOI: 10.1056/NEJMoa2034577. PMC: 7745181. PMID: 33301246.
- ↑ «Hoffnungsträger BNT162b2: Wie funktionieren mRNA-Impfstoffe?» (en alemany), 10-11-2020. [Consulta: 28 novembre 2020].
- ↑ JAMA, 324, 12, 9-2020, pàg. 1125–1127. DOI: 10.1001/jama.2020.16866. PMID: 32880613 [Consulta: free].
- ↑ bioRxiv, 08-09-2020. DOI: 10.1101/2020.09.08.280818.
- ↑ «Conditions of Authorisation for Pfizer/BioNTech COVID-19 Vaccine». Medicines & Healthcare Products Regulatory Agency, 08-12-2020.
- ↑ Office of the Commissioner. «Pfizer-BioNTech COVID-19 Vaccine». www.fda.gov. US FDA, 14-12-2020.
- ↑ Nature, 586, 7830, 10-2020, pàg. 516–527. Bibcode: 2020Natur.586..516K. DOI: 10.1038/s41586-020-2798-3. PMID: 32967006 [Consulta: free].
- ↑ «Moderna's Pipeline». Moderna. [Consulta: 28 novembre 2020].
- ↑ Dolgin, Elie Nature Biotechnology, 25-11-2020, pàg. d41587–020–00022-y. DOI: 10.1038/d41587-020-00022-y. PMID: 33239758.
- ↑ «COVID-19». CureVac. [Consulta: 21 desembre 2020].
- ↑ Cardiovascular Drugs and Therapy, 34, 6, 12-2020, pàg. 871–880. DOI: 10.1007/s10557-020-07051-4. PMC: 7441140. PMID: 32822006.
- ↑ Nature Biotechnology, 31, 10, 10-2013, pàg. 898–907. DOI: 10.1038/nbt.2682. PMC: 4058317. PMID: 24013197.
- ↑ McNamara, Megan A.; Nair, Smita K.; Holl, Eda K. Journal of Immunology Research, 2015, 2015, pàg. 794528. DOI: 10.1155/2015/794528. PMC: 4668311. PMID: 26665011.
- ↑ Verbeke, R; Lentacker, I; Wayteck, L; Breckpot, K; Van Bockstal, M Journal of Controlled Release, 266, 28-11-2017, pàg. 287–300. DOI: 10.1016/j.jconrel.2017.09.041. PMID: 28987878.
Bibliografia
modifica- Badieyan, ZS; Evans, T «Còpia arxivada». Stem Cells Translational Medicine, 8, 8, 8-2019, pàg. 833–843. Arxivat de l'original el 2022-03-08. DOI: 10.1002/sctm.18-0259. PMC: 6646692. PMID: 30891922 [Consulta: 30 abril 2021].
- NPJ Vaccines, 5, 2020, pàg. 16. DOI: 10.1038/s41541-020-0163-z. PMC: 7021756. PMID: 32128257.