สารที่ยับยั้งการสังเคราะห์โปรตีน
ลิงก์ข้ามภาษาในบทความนี้ มีไว้ให้ผู้อ่านและผู้ร่วมแก้ไขบทความศึกษาเพิ่มเติมโดยสะดวก เนื่องจากวิกิพีเดียภาษาไทยยังไม่มีบทความดังกล่าว กระนั้น ควรรีบสร้างเป็นบทความโดยเร็วที่สุด |
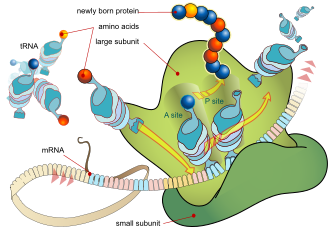
สารที่ยับยั้งการสังเคราะห์โปรตีน (อังกฤษ: Protein synthesis inhibitors) เป็นกลุ่มของสารที่หยุดหรือชะลอการเจริญเติบโตหรือการเพิ่มจำนวนของเซลล์ โดยจะออกฤทธิ์รบกวนกระบวนการการสร้างโปรตีนสายใหม่โดยตรง[1]
ถึงแม้ว่าการตีความตามคำจำกัดความดังข้างต้นทำให้สารกลุ่มนี้ดูเหมือนจะถูกจัดเป็นยาปฏิชีวนะ แต่ในทางปฏิบัติแล้ว สารกลุ่มนี้ยังหมายความรวมไปถึงสารบางชนิดที่ออกฤทธิ์ที่ระดับไรโบโซม ทั้งที่ออกฤทธิ์กับไรโบโซมโดยตรงและออกฤทธิ์รบกวนปัจจัยอื่นที่เกี่ยวข้องกับการแปรรหัสพันธุกรรม (translation factor)[2] ซึ่งเป็นการใช้ประโยชน์จากการที่โพรแคริโอตและยูแคริโอตมีโครงสร้างของไรโบโซมที่แตกต่างกัน[3]
กลไก
[แก้]โดยปกติแล้ว สารที่ออกฤทธิ์ยับยั้งการสังเคราะห์โปรตีนนั้นจะออกฤทธิ์ในกระบวนการแปรรหัสพันธุกรรมของเซลล์โพรคาริโอต (Prokaryotic translation) ที่ลำดับขั้นตอนที่แตกต่างกันออกไป เช่น ขั้นเริ่มต้น, ขั้นต่อสาย (รวมถึง ขั้นตอนการเข้าจับของอะมิโนเอซิลทีอาร์เอ็นเอ, การตรวจสอบลำดับของนิวคลีโอไทด์ในสายดีเอ็นเอ (proofreading), การขนส่งหมู่เปปทิดิล, และ การย้ายตำแหน่ง) และขั้นหยุด
ขั้นต้น
[แก้]- ไรฟามัยซิน จะยับยั้งการถอดรหัสดีเอ็นเอของเซลล์โพรคาริโอตไปเป็นเอ็มอาร์เอ็นเอ โดยการจับกับ DNA-dependent RNA polymerase ตำแหน่งหน่วยย่อยบีตา (beta-subunit).
ขั้นเริ่มต้น
[แก้]- ไลนิโซลิด จะออกฤทธิ์ยับยั้งกระบวนการสังเคราะห์โปรตีนในขั้นเริ่มต้นของกระบวนการ[4] ถึงแม้ว่ากลไกกการออกฤทธิ์ของยานี้จะยังไม่สามารถทราบได้อย่างเด่นชัดเท่าใดนัก แต่คาดว่ายาดังกล่าวจะทำให้เอ็มอาร์เอ็นเอและไรโบโซมไม่สามารถรวมกันเป็น สารเซิงซ้อนแรกเริ่ม (initial complex) ได้[5]
ขั้นการรวมกันของไรโบโซม
[แก้]- นีโอมัยซิน ออกฤทธิ์ขัดขวางขั้นตอนการรวมกันของไรโบโซม (ribosome assembly) โดยจับกับหน่วยย่อย 30 เอสของไรโบโซมของเซลล์โพรคาริโอต[6]
ขั้นตอนการเข้าจับของอะมิโนเอซิลทีอาร์เอ็นเอ
[แก้]- เตตราไซคลีน และไทกีไซคลีน[7] (ยากลุ่มไกลซิลไซคลีน ซึ่งเป็นกลุ่มย่อยของเตตราไซคลีน) จะจับกับ A site บนไรโบโซม ทำให้อะมิโนเอซิลทีอาร์เอ็นเอน ไม่สามารถเข้าจับกับตำแหน่งดังกล่าวได้
ขั้นการตรวจสอบลำดับของนิวคลีโอไทด์
[แก้]- อะมิโนไกลโคไซด์ เป็นยาปฏิชีวนะที่ออกฤทธิ์ขัดขวางการตรวจสอบลำดับของนิวคลีโอไทด์ในสายดีเอ็นเอ ผลที่เกิดจากการขัดขวางกระบวนการนี้จะทำให้การสังเคราะห์โปรตีนผิดพลาด และทำให้กระบวนการสังเคราะห์โปรตีนนั้นเข้าสู่ขั้นหยุดเร็วกว่าที่ควรจะเป็น[8]
ขั้นการขนส่งหมู่เปปทิดิล
[แก้]- คลอแรมเฟนิคอล ออกฤทธิ์ยับยั้งขั้นตอนการขนส่งหมู่เปปทิดิลในขั้นต่อสาย บนหน่วยย่อย 50 เอสของไรโบโซมทั้งในเซลล์แบคทีเรียและไมโทคอนเดรีย
- แมคโครไลด์ (ทั้งนี้ยังยับยั้งการย้ายตำแหน่งของไรโบโซม[9] และกระบวนการอื่นอีกหลายกระบวนการ) จะจับกับหน่วยย่อย 50 เอสของไรโบโซม เพื่อยับยั้งการขนส่งหมู่เปปทิดิล
- ควินูปริสติน/ดาลโฟปริสติน มีผลเสริมการออกฤทธิ์ซึ่งกันและกัน (synergic effect) โดยควินูปริสตินจะจับกับหน่วยย่อย 50 เอสของไรโบโซม เพื่อยับยั้งการขนส่งหมู่เปปทิดิล และป้องกันไม่ให้เกิดขั้นต่อสาย ทำให้การสายพอลีเพปไทด์ที่ถูกสร้างได้นั้นไม่สมบูรณ์[10] ส่วนดาลโฟปริสตินจะช่วยเพิ่มประสิทธิภาพในการจับตำแหน่งเป้ามหายของควินูปริสติน[10]
- จีนีติซิน หรือ G418 ออกฤทธิ์ยับยั้งที่ขั้นต่อสาย ทั้งในไรโบโซมของโพรคาริโอตและยูคาริโอต[11]
การย้ายตำแหน่งของไรโบโซม
[แก้]- แมคโครไลด์,[9] คลินดามัยซิน[12] และ อะมิโนไกลโคไซด์[8] (ยาทั้ง 3 ชนิด/กลุ่มนี้ ยังสามารถออกฤทธิ์ยับยั้งขั้นตอนอื่นได้อีกหลายขั้นตอน) มีหลักฐานเชิงประจักษ์ที่ยืนยันได้ว่าสามารถออกฤทธิ์ยับยั้งขั้นตอนการย้ายตำแหน่งได้
- กรดฟูซิดิค ป้องกันไม่ให้ไรโบโซมนำ elongation factor G (EF-G) วนกลับมาใช้ใหม่
- ไรซิน ยับยั้งการต่อสาย โดยส่งผลให้เกิดการเปลี่ยนแปลงของอาร์อาร์เอ็นเอ ของหน่วยย่อย 60 เอสของไรโบโซมในยูคาริโอต[13][14]
ขั้นหยุด
[แก้]- แมคโครไลด์[15][16] และ คลินดามัยซิน[15][16] (ทั้ง 2 ชนิดยังมีกลไกการออกฤทธิ์อื่นในการออกฤทธิ์) ทำให้เปปทิดิลทีอาร์เอ็นเอ (peptidyl-tRNA) แยกตัวออกจากไรโบโซมเร็วกว่าปกติ
- พิวโรมัยซิน ซึ่งมีโครงสร้างคล้ายกับ ไทโรซินิลอะมิโนเอซิลทีอาร์เอ็นเอ จะเข้าจับกับตำแหน่ง A site บนไรโบโซมด้วยพันธะเพปไทด์ อย่างไรก็ตาม พิวโรมัยซินจะไม่ส่งผลต่อการย้ายตำแหน่งของไรโบโซม โดยหลังจากจับกับ A site แล้วยาดังกล่าวจะแยกตัวออกจากไรโบโซมอย่างรวดเร็ว ส่งผลให้การสังเคราะห์โปรตีนนั้นเข้าสู่ขั้นหยุดเร็วกว่าที่ควรจะเป็น
- สเตรปโตกรามิน เป็นยาปฏิชีวนะอีกชนิดหนึ่งที่ทำให้การสังเคราะห์สายพอลิเปปไทด์สิ้นสุดเร็วกว่าปกติ[17]
กลไกไม่จำเพาะ
[แก้]ตำแหน่งออกฤทธิ์
[แก้]ยาต่อไปนี้เป็นยาที่ออกฤทธิ์ยับยั้งการสังเคราะห์โปรตีนโดยการเข้าจับกับหน่วยย่อย 30 เอสของไรโบโซม:
ยาต่อไปนี้เป็นยาที่ออกฤทธิ์ยับยั้งการสังเคราะห์โปรตีนโดยการเข้าจับกับหน่วยย่อย 50 เอสของไรโบโซม:
- คลอแรมเฟนิคอล[17]
- อิริโทรมัยซิน[17]
- คลินดามัยซิน[17]
- ไลนิโซลิด[17] (กลุ่มออกซาโซลิไดโอน)
- เทลิโทรมัยซิน[17]
- สเตรปโตกรามิน[17]
- เรตาพามูลิน[18]
ดูเพิ่ม
[แก้]อ้างอิง
[แก้]- ↑ "Definition: protein synthesis inhibitor from Online Medical Dictionary".
- ↑ "7.344 Antibiotics, Toxins, and Protein Engineering, Spring 2007". MIT OpenCourseWare.
- ↑ Berg JM, Tymoczko JL, Stryer L. (2002). Eukaryotic Protein Synthesis Differs from Prokaryotic Protein Synthesis Primarily in Translation Initiation. Biochemistry. Vol. 5th Ed. W H Freeman.
{{cite book}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Swaney SM, Aoki H, Ganoza MC, Shinabarger DL (December 1998). "The Oxazolidinone Linezolid Inhibits Initiation of Protein Synthesis in Bacteria". Antimicrob. Agents Chemother. 42 (12): 3251–3255. PMC 106030. PMID 9835522.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Skripkin E, McConnell TS, DeVito J และคณะ (October 2008). "Rχ-01, a New Family of Oxazolidinones That Overcome Ribosome-Based Linezolid Resistance". Antimicrobial Agents and Chemotherapy. 52 (10): 3550–3557. doi:10.1128/AAC.01193-07. PMC 2565890. PMID 18663023.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Mehta, Roopal; Champney, W. Scott (2003). "Neomycin and Paromomycin Inhibit 30S Ribosomal Subunit Assembly in Staphylococcus aureus". Current Microbiology. 47 (3): 237–43. doi:10.1007/s00284-002-3945-9. PMID 14570276.
- ↑ Slover CM, Rodvold KA, Danziger LH (June 2007). "Tigecycline: a novel broad-spectrum antimicrobial". Ann Pharmacother. 41 (6): 965–972. doi:10.1345/aph.1H543. PMID 17519296. สืบค้นเมื่อ 2009-12-19.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 8.0 8.1 Flavio Guzmán (12 August 2008). "Protein synthesis inhibitors: aminoglycosides mechanism of action animation. Classification of agents". Pharmamotion. คลังข้อมูลเก่าเก็บจากแหล่งเดิมเมื่อ 12 March 2010. สืบค้นเมื่อ 2018-01-07.
- ↑ 9.0 9.1 Protein synthesis inhibitors: macrolides mechanism of action animation. Classification of agents เก็บถาวร 2008-12-26 ที่ เวย์แบ็กแมชชีน Pharmamotion. Author: Gary Kaiser. The Community College of Baltimore County. Retrieved on July 31, 2009
- ↑ 10.0 10.1 Page 212 in: Title: Hugo and Russell's pharmaceutical microbiology Authors: William Barry Hugo, Stephen P. Denyer, Norman A. Hodges, Sean P. Gorman Edition: 7, illustrated Publisher: Wiley-Blackwell, 2004 ISBN 0-632-06467-6 Length: 481 pages
- ↑ "Geneticin". Thermo Fisher Scientific.
- ↑ Wisteria Lane cases --> CLINDAMYCIN เก็บถาวร 2012-07-18 ที่ archive.today University of Michigan. Retrieved on July 31, 2009
- ↑ Leonard JE, Grothaus CD, Taetle R (October 1988). "Ricin binding and protein synthesis inhibition in human hematopoietic cell lines". Blood. 72 (4): 1357–1363. PMID 3167211.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ Terao K, Uchiumi T, Endo Y, Ogata K (June 1988). "Ricin and alpha-sarcin alter the conformation of 60S ribosomal subunits at neighboring but different sites". Eur. J. Biochem. 174 (3): 459–463. doi:10.1111/j.1432-1033.1988.tb14120.x. PMID 3391162.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์)[ลิงก์เสีย] - ↑ 15.0 15.1 Menninger JR (1995). "Mechanism of inhibition of protein synthesis by macrolide and lincosamide antibiotics". J Basic Clin Physiol Pharmacol. 6 (3–4): 229–250. doi:10.1515/JBCPP.1995.6.3-4.229. PMID 8852269.
- ↑ 16.0 16.1 Tenson T, Lovmar M, Ehrenberg M (July 2003). "The mechanism of action of macrolides, lincosamides and streptogramin B reveals the nascent peptide exit path in the ribosome". J. Mol. Biol. 330 (5): 1005–1014. doi:10.1016/S0022-2836(03)00662-4. PMID 12860123.
{{cite journal}}: CS1 maint: uses authors parameter (ลิงก์) - ↑ 17.0 17.1 17.2 17.3 17.4 17.5 17.6 17.7 17.8 Levinson, Warren (2008). Review of medical microbiology and immunology. New York: McGraw-Hill Medical. ISBN 978-0-07-149620-9.
- ↑ 18.0 18.1 Drugbank.ca > Showing drug card for Retapamulin (DB01256) Update Date: 2009-06-23